天然氨基酸逆袭阿尔茨海默病!Neurochem Int:口服精氨酸瓦解 β 淀粉样斑块,低成本疗法有望快速临床转化
来源:生物谷原创 2025-11-26 10:31
这项研究通过药物重定位策略,为 AD 治疗提供了一种经济有效、易于大规模推广的新方向。
阿尔茨海默病(AD)是全球最主要的痴呆症类型,目前已影响超 5000 万人,随着人口老龄化加剧,它正成为重大公共卫生挑战。这种疾病的核心病理特征是大脑中 β 淀粉样蛋白(Aβ)异常聚集形成斑块,以及 tau 蛋白过度磷酸化形成神经原纤维缠结,最终导致神经元损伤和认知功能衰退。
尽管近年来靶向 Aβ 的单克隆抗体药物(如 lecanemab、donanemab)已获批上市,但它们疗效有限,不仅价格高昂,还可能引发淀粉样蛋白相关影像学异常(ARIA)等副作用,让许多患者难以负担和耐受。因此,开发安全、低成本、易获取的治疗方案,成为全球科研界的迫切需求。
发表于《Neurochemistry International》期刊的一项新研究,为 AD 治疗带来了突破性希望:近畿大学及合作机构的研究人员发现,口服精氨酸——一种天然存在的氨基酸,同时也是临床认可的安全化学伴侣,能显著抑制 Aβ 聚集,减轻其毒性作用,在多种 AD 动物模型中展现出强效的神经保护效果。
该研究由近畿大学医学院神经内科的藤井佳奈子、永井良隆教授,以及近畿大学生命科学研究所的竹内俊秀副教授共同领导,其核心优势在于精氨酸的安全性和可及性,为 AD 治疗的快速临床转化奠定了基础。

研究团队首先通过体外实验验证了精氨酸的抗 Aβ 聚集能力。他们将 Aβ42 肽段在 37℃下孵育,发现随着孵育时间延长,Aβ42 会逐渐聚集,而精氨酸能以浓度依赖的方式抑制这一过程——当精氨酸浓度达到 1mM 时,Aβ42 聚集量减少 80%,效果媲美已知的抗聚集分子 EGCG。电镜观察进一步显示,未经处理的 Aβ42 会形成长纤维状聚集物,而精氨酸处理后,这些纤维明显缩短、断裂,难以形成具有毒性的淀粉样结构,直接证明了精氨酸对 Aβ 聚集的抑制作用。
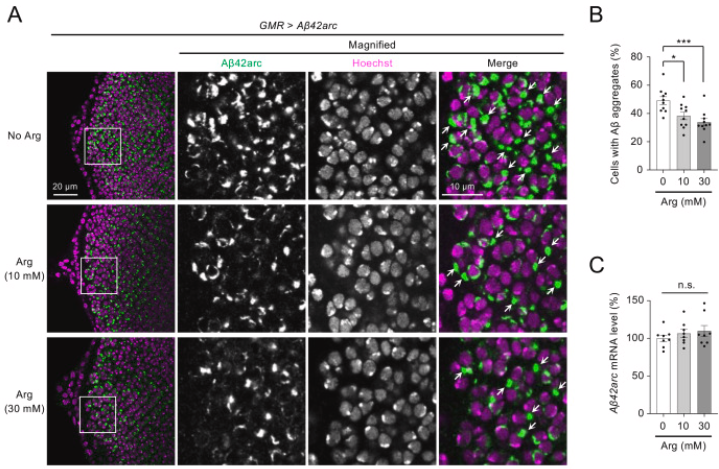
基于体外实验的积极结果,研究团队在两种经典 AD 模型中进行了体内验证。第一种是表达带 Arctic 突变(E22G)Aβ42 的果蝇模型,这种突变会导致 Aβ42 更易聚集,进而引发果蝇眼部组织损伤和眼萎缩。
口服给予精氨酸后,果蝇幼虫眼盘内的 Aβ42 沉积剂量依赖地减少,且不影响 Aβ42 转基因的表达;成年果蝇的眼部萎缩症状也得到显著改善,10mM 和 30mM 剂量的精氨酸能有效维持眼部正常大小,证明精氨酸能在体内抑制 Aβ 聚集并减轻其毒性。
第二种是更贴近人类 AD 病理的 AppNL-G-F 基因敲入小鼠模型,这些小鼠携带瑞典、北极、Beyreuther/Iberian 三个家族性 AD 突变,会随年龄增长自然出现 Aβ 斑块沉积和行为异常。研究人员从小鼠 5 周龄开始,在饮用水中添加 6% 精氨酸(人体等效剂量约 940mg/kg/ 天,约为日本临床获批最大剂量的两倍,且已证实对野生型小鼠无不良影响),持续给药至 6 个月和 9 个月。
结果显示,6 个月时,精氨酸处理组小鼠的大脑皮层和海马区——AD 病理损伤最严重的区域,Aβ 斑块的数量和面积均显著减少,尤其是致密核心斑块(淀粉样聚集的成熟形式)减少更为明显;生化分析表明,大脑中不溶性 Aβ42(具有强毒性的聚集形式)水平大幅降低,而可溶性 Aβ42 无明显变化,说明精氨酸主要抑制 Aβ 的聚集过程,而非影响其产生。
更令人振奋的是,精氨酸的益处不止于减少 Aβ 沉积。在 9 个月大的 AppNL-G-F 小鼠中,接受精氨酸治疗的小鼠在 Y 迷宫测试中表现更佳,自发活动的总距离和臂进入次数明显增加,行为异常得到改善;同时,大脑中与神经炎症相关的促炎细胞因子(IL-1β、IL-6、TNF)基因表达水平显著降低——神经炎症是 AD 进展的关键推手,能加剧神经元损伤,这一发现表明精氨酸还具有抗炎作用,能全面改善 Aβ 介导的神经病理表型。
值得强调的是,精氨酸并非全新化合物,它已在临床上用于治疗尿素循环缺陷、线粒体肌病等疾病,且在脊髓小脑性共济失调 6 型(SCA6)的 2 期临床试验中展现出良好的安全性和潜在疗效。作为化学伴侣,精氨酸还能抑制多聚谷氨酰胺蛋白、α-突触核蛋白等多种易错误折叠蛋白的聚集,意味着它不仅对 AD 有治疗潜力,还可能适用于帕金森病、肌萎缩侧索硬化等多种神经退行性疾病。
研究人员同时提醒,实验中使用的精氨酸剂量和给药方案是为科研设计的,与市面上的膳食补充剂不同,不能直接替代治疗;且目前研究仍处于动物实验阶段,AppNL-G-F 小鼠未完全复刻人类 AD 的所有病理特征(如 tau 缠结和明显神经元丢失), 散发性 AD 患者是否能获得同样效果,还需进一步临床研究验证。但鉴于精氨酸口服方便、成本低廉、安全性高且具有良好的脑渗透性,它有望绕过传统药物开发的早期障碍,快速进入临床转化阶段。
这项研究通过药物重定位策略,为 AD 治疗提供了一种经济有效、易于大规模推广的新方向。它不仅深化了我们对 Aβ 聚集机制的理解,更让全球数千万 AD 患者看到了低成本治疗的希望。未来,随着临床研究的推进,精氨酸有望成为 AD 预防和治疗的重要选择,甚至为其他蛋白质错误折叠相关疾病的治疗提供借鉴,真正实现 “老药新用” 的临床价值。(生物谷Bioon.com)
参考文献:
Kanako Fujii et al, Oral administration of arginine suppresses Aβ pathology in animal models of Alzheimer's disease. Neurochemistry International, 2025; 191: 106082 DOI: 10.1016/j.neuint.2025.106082.
版权声明
本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->





